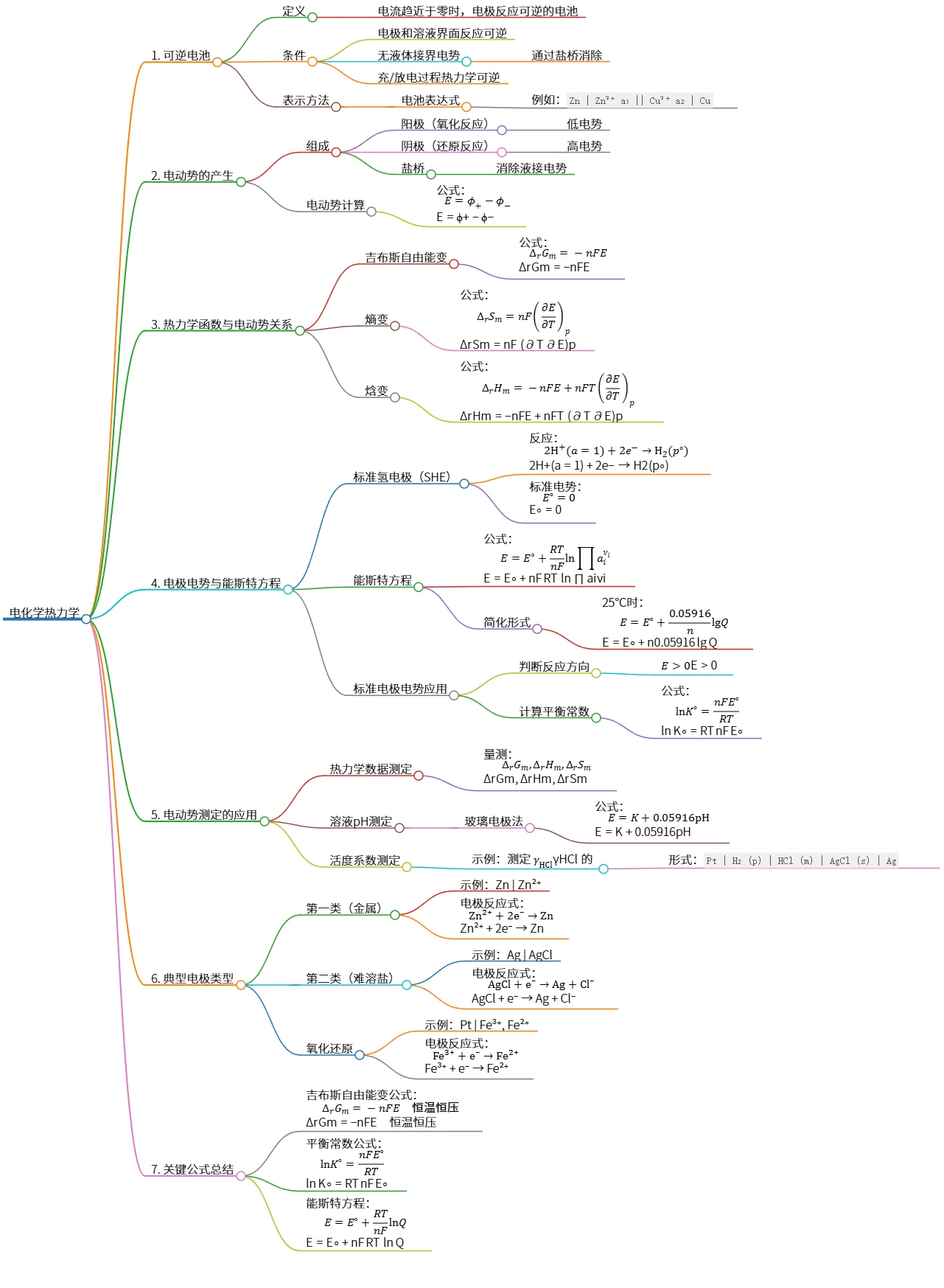
电化学热力学:可逆电池与电动势的关系分析
该思维导图概述了电化学热力学的基本概念,包括可逆电池的定义和条件、电动势产生的组成及计算、热力学函数与电动势的关系、能斯特方程及其应用,以及电动势测定的方法和典型电极类型的示例。此外,还总结了关键公式,为理解电化学过程提供了理论基础。
源码
# 电化学热力学
## 1. 可逆电池
- 定义
- 电流趋近于零时,电极反应可逆的电池
- 条件
- 电极和溶液界面反应可逆
- 无液体接界电势
- 通过盐桥消除
- 充/放电过程热力学可逆
- 表示方法
- 电池表达式
- 例如:`Zn | Zn²⁺ a₁ || Cu²⁺ a₂ | Cu`
## 2. 电动势的产生
- 组成
- 阳极(氧化反应)
- 低电势
- 阴极(还原反应)
- 高电势
- 盐桥
- 消除液接电势
- 电动势计算
- 公式:$$E = \phi_+ - \phi_-$$
## 3. 热力学函数与电动势关系
- 吉布斯自由能变
- 公式:$$\Delta_r G_m = -nFE$$
- 熵变
- 公式:$$\Delta_r S_m = nF\left(\frac{\partial E}{\partial T}\right)_p$$
- 焓变
- 公式:$$\Delta_r H_m = -nFE + nFT\left(\frac{\partial E}{\partial T}\right)_p$$
## 4. 电极电势与能斯特方程
- 标准氢电极(SHE)
- 反应:$$2\text{H}^+ (a=1) + 2e^- \rightarrow \text{H}_2 (p^\circ)$$
- 标准电势:$$E^\circ=0$$
- 能斯特方程
- 公式:$$E = E^\circ + \frac{RT}{nF} \ln \prod a_i^{\nu_i}$$
- 简化形式
- 25℃时:$$E = E^\circ + \frac{0.05916}{n} \lg Q$$
- 标准电极电势应用
- 判断反应方向
- $E > 0$ 自发
- 计算平衡常数
- 公式:$$\ln K^\circ = \frac{nFE^\circ}{RT}$$
## 5. 电动势测定的应用
- 热力学数据测定
- 量测:$$\Delta_r G_m, \Delta_r H_m, \Delta_r S_m$$
- 溶液pH测定
- 玻璃电极法
- 公式:$$E = K + 0.05916 \text{pH}$$
- 活度系数测定
- 示例:测定 $\gamma_{\text{HCl}}$ 的电池
- 形式:`Pt | H₂ (p) | HCl (m) | AgCl (s) | Ag`
## 6. 典型电极类型
- 第一类(金属)
- 示例:Zn | Zn²⁺
- 电极反应式:$$\text{Zn²⁺ + 2e⁻ → Zn}$$
- 第二类(难溶盐)
- 示例:Ag | AgCl
- 电极反应式:$$\text{AgCl + e⁻ → Ag + Cl⁻}$$
- 氧化还原
- 示例:Pt | Fe³⁺, Fe²⁺
- 电极反应式:$$\text{Fe³⁺ + e⁻ → Fe²⁺}$$
## 7. 关键公式总结
- 吉布斯自由能变公式:$$\Delta_r G_m = -nFE \quad \text{恒温恒压}$$
- 平衡常数公式:$$\ln K^\circ = \frac{nFE^\circ}{RT}$$
- 能斯特方程:$$E = E^\circ + \frac{RT}{nF} \ln Q$$
图片