高中热化学的基本概念及其重要性解析
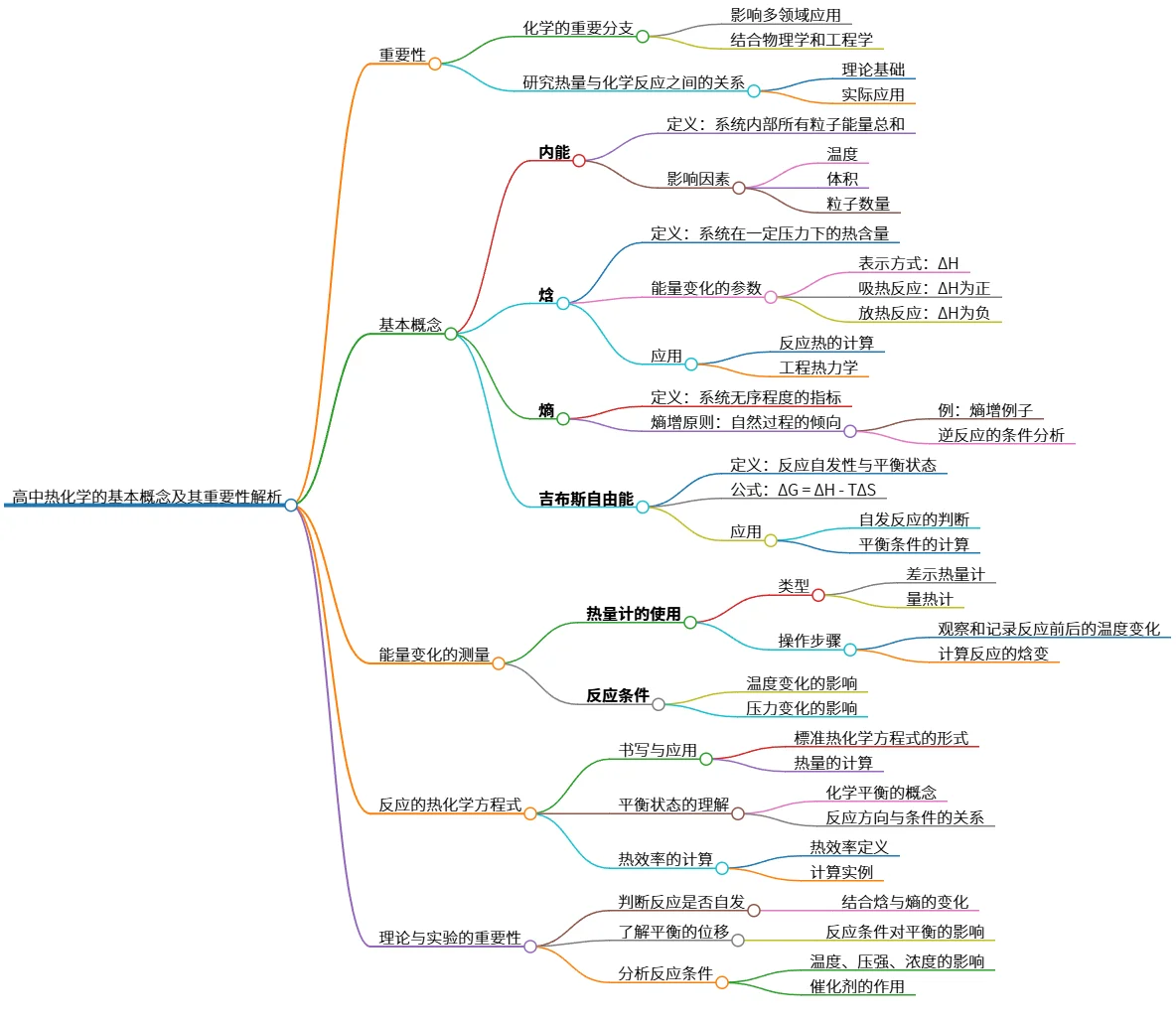
该思维导图概述了高中热化学的基本概念和重要性,强调了内能、焓、熵和吉布斯自由能等核心概念。它介绍了能量变化的测量方法,如热量计的使用,以及反应的热化学方程式的书写与应用。此外,思维导图还指出理论与实验在判断反应自发性、理解平衡状态和分析反应条件中的重要性。
源码
# 高中热化学的基本概念及其重要性解析
## 重要性
- 化学的重要分支
- 影响多领域应用
- 结合物理学和工程学
- 研究热量与化学反应之间的关系
- 理论基础
- 实际应用
## 基本概念
- **内能**
- 定义:系统内部所有粒子能量总和
- 影响因素
- 温度
- 体积
- 粒子数量
- **焓**
- 定义:系统在一定压力下的热含量
- 能量变化的参数
- 表示方式:ΔH
- 吸热反应:ΔH为正
- 放热反应:ΔH为负
- 应用
- 反应热的计算
- 工程热力学
- **熵**
- 定义:系统无序程度的指标
- 熵增原则:自然过程的倾向
- 例:熵增例子
- 逆反应的条件分析
- **吉布斯自由能**
- 定义:反应自发性与平衡状态
- 公式:ΔG = ΔH - TΔS
- 应用
- 自发反应的判断
- 平衡条件的计算
## 能量变化的测量
- **热量计的使用**
- 类型
- 差示热量计
- 量热计
- 操作步骤
- 观察和记录反应前后的温度变化
- 计算反应的焓变
- **反应条件**
- 温度变化的影响
- 压力变化的影响
## 反应的热化学方程式
- 书写与应用
- 標准热化学方程式的形式
- 热量的计算
- 平衡状态的理解
- 化学平衡的概念
- 反应方向与条件的关系
- 热效率的计算
- 热效率定义
- 计算实例
## 理论与实验的重要性
- 判断反应是否自发
- 结合焓与熵的变化
- 了解平衡的位移
- 反应条件对平衡的影响
- 分析反应条件
- 温度、压强、浓度的影响
- 催化剂的作用
图片